4月9日,人福醫(yī)藥發(fā)布公告稱,控股子公司宜昌人福藥業(yè)收到FDA關于布洛芬片的批準文號,意味著可以生產并在美國市場銷售該產品。人福醫(yī)藥在制劑出口海外的賽道上碩果累累,目前已拿下的ANDA文號超過90個。
表1:人福醫(yī)藥最新獲批產品情況
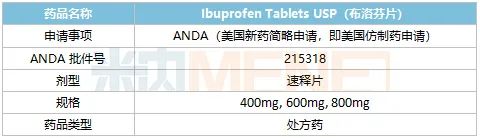
來源:公司公告
布洛芬片適用于緩解輕至中度疼痛如頭痛、關節(jié)痛、偏頭痛、牙痛、肌肉痛、神經痛、痛經,也適用于普通感冒或流行性感冒引起的發(fā)熱。
據悉,宜昌人福于2021年提交布洛芬片的ANDA申請,累計研發(fā)投入約為140萬美元。公司表示,本次布洛芬片獲得美國FDA批準文號標志著宜昌人福具備了在美國市場銷售該產品的資格,將對公司拓展美國仿制藥市場帶來積極的影響,公司后續(xù)將積極推進該產品在美國市場的上市準備工作。
宜昌人福的布洛芬片在國內市場也有銷售,公司于2017年開展一致性評價研究,2019年進行生物等效性研究,2019年8月申報并于2020年9月獲批過評。該產品順利中標第四批國采,隨后銷售額快速增長,米內網數據顯示,2021上半年在中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機構)終端布洛芬片的企業(yè)格局中,宜昌人福藥業(yè)一躍成為TOP4企業(yè),市場份額高達6.05%。
表2:人福醫(yī)藥已獲得的ANDA文號情況
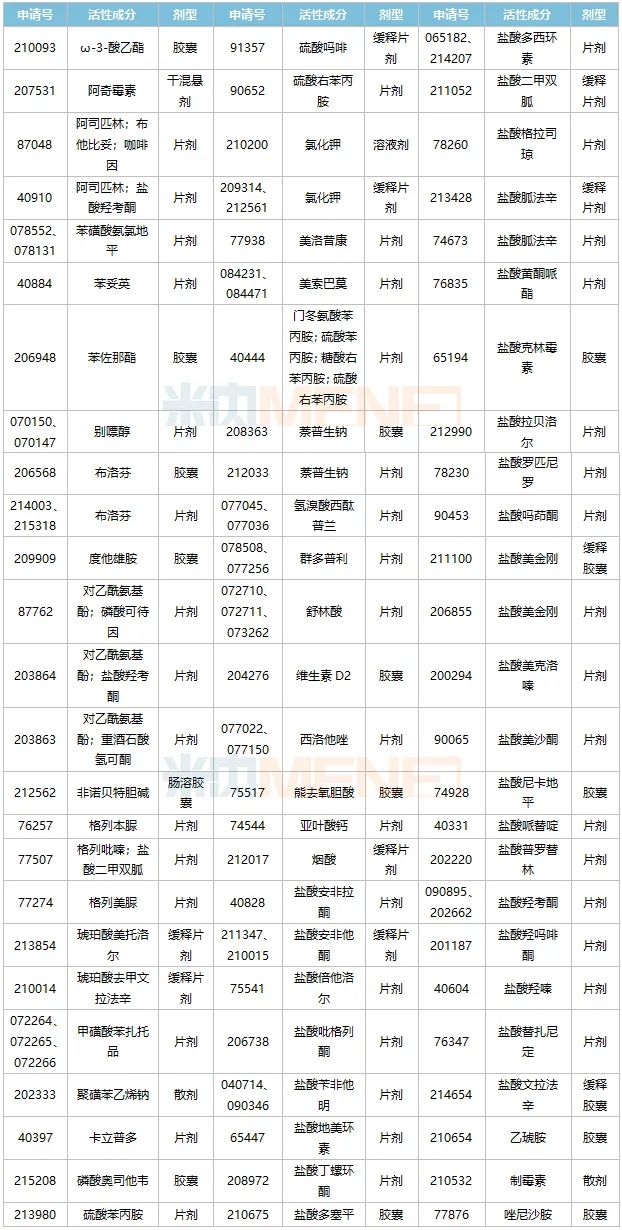
來源:米內網全球上市藥物數據庫
數據顯示,人福醫(yī)藥目前獲得的ANDA文號超過90個,涉及產品(活性成分+劑型)達75個,在制劑出口海外的賽道上,人福醫(yī)藥一直處于領跑地位。
來源:公司公告、米內網數據庫
注:ANDA數據統(tǒng)計截至4月6日,如有疏漏,歡迎指正!



